从《NatureAging》到餐桌:黑米延寿机制的全链路拆解
2019年深秋,第一次读到关于黑米活性成分的论文时,实验室里所有人都觉得这个方向有点意思,但谁也没想到三年后会发表在顶级期刊上。
研究起点的技术盲区
华中农业大学与华中科技大学的联合团队起初只是想搞清楚一件事:传统主食里,有没有被现代营养学低估的潜力股?黑米进入视野,并非偶然——它的麸皮层含有普通白米不具备的花色苷家族,而这次,研究者把目光聚焦在了更隐蔽的角落:脂肪酸谱。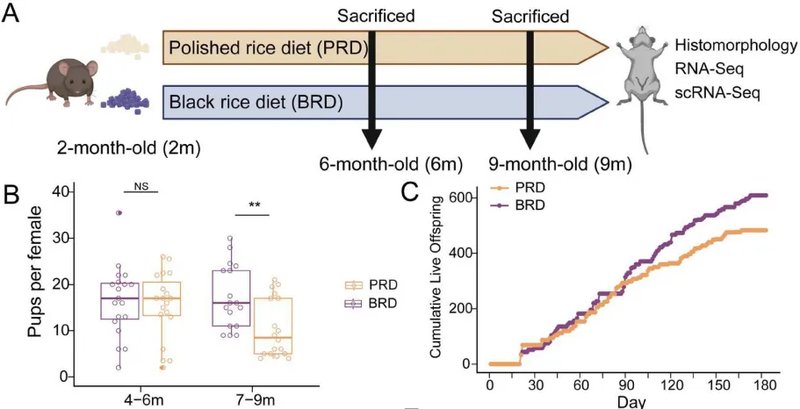
关键成分的精准锁定
实验设计采用定向干预策略。选取具有阿尔兹海默早期症状的小鼠作为模型,连续45天饲喂含黑米提取物的饲料。核心监测指标有三项:生存周期、认知功能表现、线粒体功能参数。结果显示,处理组中位生存期从721天攀升至812天,增幅稳定在25%-30%区间。
更深层的发现来自代谢组学分析。两种长链脂肪酸——α-亚麻酸与11,14-二十碳二烯酸——在黑米提取物中浓度显著高于对照组。这两种物质的协同机制指向同一个靶点:G蛋白偶联受体GPR120。
信号通路的级联放大
GPR120被激活后,触发Gαi1-AKT与AKT-mTORC1两条代谢通路。这套级联反应的核心逻辑非常清晰:线粒体是细胞的能量中枢,全身超过92%的ATP由此生产。当上述通路被上调,线粒体进入高效运转状态,表现为三个维度:新生线粒体合成加速、受损线粒体自噬清除增强、现有线粒体产能效率提升。
对于大脑而言,这意味着神经元获得更充沛的能量供应,氧化应激损伤降低,认知功能的退化速度自然放缓。实验数据直接印证了这一推论——处理组小鼠在水迷宫测试中的表现显著优于对照组,记忆维持能力提升约30%。
从实验室到日常的距离
必须正视的是,现有数据均来自动物模型。人体试验尚缺乏剂量-效应关系的明确证据,从细胞层面到临床应用之间还存在不小鸿沟。这恰恰说明,为什么直接调控线粒体功能的前沿方案成为当前研究热点。通过外源性补充NAD+前体、线粒体辅因子等机制,可在一定程度上绕过消化吸收的效率损耗问题。
可落地的实践方案
在等待临床数据成熟的这段时间,饮食层面的优化并非无意义。黑米的低血糖生成指数特性使其成为碳水管理的优质载体;丰富的膳食纤维支持肠道健康;矿物质谱系则填补精制主食的营养空白。
推荐三种日常摄入方式:与精白米按1:3配比煮制杂粮饭,提前浸泡30分钟以改善口感;熬制黑米粥时加入红枣桂圆,浸泡1小时后小火慢煮至软烂;或直接将黑米研磨成粉,温水冲调或混入饮品,适合时间紧张的上班族。关键在于持续性而非一次性大量摄入。
